Über LHON
LHON im Überblick
Was genau ist LHON?
LHON ist die Abkürzung für Lebersche Hereditäre Optikus-Neuropathie. Der Name geht auf den deutschen Augenarzt Theodor Carl Gustav von Leber zurück. Er beschrieb die Erkrankung erstmalig 1871 bei vier Familien.
LHON ist eine seltene, erblich bedingte Augenerkrankung. Bei dieser Erkrankung sind Zellen in der Netzhaut in ihrer Funktion betroffen. LHON kann zu einer schweren Einschränkung des Sehvermögens führen.
LHON und deren Häufigkeit
Die Schwere der Einschränkung kann von Patient*in zu Patient*in unterschiedlich ausgeprägt sein.1,2 1,9 bis 3,2 von 100.000 Personen sind im Durchschnitt von ihr betroffen. Jedes Jahr erkrankt weltweit von 1.000.000 Menschen vermutlich einer neu an LHON.3,4 In Deutschland werden schätzungsweise pro Jahr 30 bis 80 neue LHON-Diagnosen gestellt. In 80 % der Fälle sind junge Männer zwischen 15 und 35 Jahren betroffen.5 Frauen erkranken in der Regel seltener an der Augenkrankheit6 – und das eher später im Leben.7,8
Ursachen und Entstehungen von LHON
Die Ursache für LHON ist ein Gendefekt, eine kleine Veränderung an bestimmten Stellen im Erbgut.2 Das Erbgut wird auch DNA oder DNS genannt; Veränderungen des Erbguts nennt man Mutationen. Dieser Gendefekt bzw. die Mutation führt zu einer Funktionsstörung der Mitochondrien, den Kraftwerken unserer Zellen. Eine Besonderheit von Mitochondrien ist, dass sie eine kleine Menge eigenes Erbgut besitzen, die sogenannte mitochondriale DNA.
Je nachdem, ob der Gendefekt in der mitochondrialen DNA oder in dem Erbgut der Zelle - der nukleären DNA - auftritt, wird LHON unterschiedlich vererbt.2,9
Mutationen in der mitochondrialen DNA
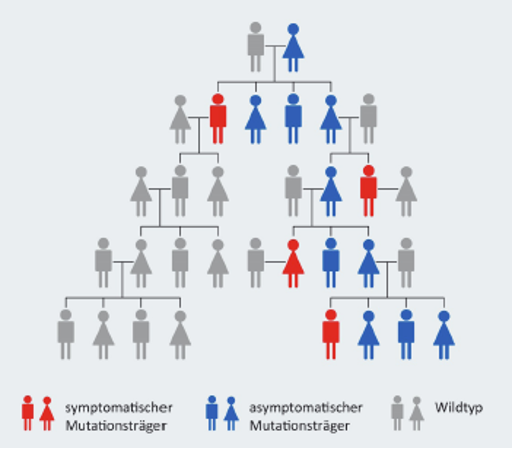
Der mitochondriale DNA-Anteil wird ausschließlich von der Mutter weitergegeben. Deshalb können auch Mutationen in der mitochondrialen DNA nur durch die Mutter vererbt werden. Männer können Mutationen in der mitochondrialen DNA nicht an ihre Kinder weitergeben. Dabei ist es egal, ob der Mann nur Mutationsträger ist oder auch an Symptomen von LHON leidet.
Die Mehrzahl (ungefähr 90 %) der LHON-Patient*innen weist eine von drei mitochondrialen DNA-Mutationen auf.6 Die häufigste Mutation ist m.11778G>A (ca. 60–75 % der Fälle), gefolgt von m.14484T>C (ca. 10–20 %) und m.3460G>A (ca. 10–20 %).10
Mutationen in der nukleären DNA
Laut wissenschaftlichen Erkenntnissen aus dem Jahr 2021 zufolge können auch Mutationen in der nukleären DNA für das Auftreten von LHON verantwortlich sein.9 Auch diese Mutationen führen zu einem Defekt in den Mitochondrien. Für Betroffene und ihre Angehörigen ist es wichtig zu wissen, dass die nukleären DNA-Mutationen sowohl von der Mutter als auch vom Vater an die Kinder weitergegeben werden können.9 Man spricht in diesem Fall auch von autosomal-rezessiver LHON.9
Vom Gendefekt zur Erkrankung
Die Mutationen, die LHON verursachen können, liegen meistens in der mitochondrialen DNA. Die Mitochondrien sind ein Bestandteil unserer Körperzellen und werden als die „Kraftwerke“ der Zellen bezeichnet, weil sie einen Großteil der Energie produzieren. Das geschieht in der sogenannten mitochondrialen Atmungskette. In ihr werden Elektronen über eine Reihe verschiedener Eiweiße (sogenannte Komplexe) transportiert, um am Ende Energie zu produzieren. Das Problem bei LHON: Einer der Komplexe ist reduziert in seiner Funktion und gibt die Elektronen nicht richtig weiter. Dadurch wird weniger Energie gebildet.11,12
Bei LHON hat diese Funktionsstörung vor allem Auswirkungen auf die Nervenzellen in der Netzhaut des Auges (die retinalen Ganglienzellen). Sie sind dafür zuständig, optische Signale vom Auge ans Gehirn weiterzuleiten. Werden sie mit zu wenig Energie versorgt, gehen sie in eine Art Ruhemodus, wodurch es zu Beeinträchtigungen beim Sehen kommen kann. Einige dieser Zellen können im Verlauf auch absterben.12 Die Dicke der Nervenzellschicht der Netzhaut nimmt dadurch mit der Zeit ab.
Bei einer speziellen Untersuchung der Netzhaut, der optischen Kohärenztomographie, lässt sich dies sichtbar machen. Besonders die Ganglienzellen in der zentralen Netzhaut sind betroffen, sodass es vor allem in der Mitte des Gesichtsfeldes zu einer Sehminderung kommt.6
Nicht alle Mutationsträger*innen entwickeln zwingend eine LHON-Erkrankung. Ob LHON auftritt muss nicht allein von der genetischen Veranlagung abhängig sein. Auch Triggerfaktoren wie Nikotin- und Alkoholkonsum sowie Verletzungen im Kopfbereich und Stress können für den Ausbruch eine Rolle spielen. 1,6,13,14
Was bei LHON noch wichtig ist
Lesen Sie in weiteren Beiträgen, wie LHON diagnostiziert werden kann und welche Symptome die Erkrankung mit sich bringt. Daneben finden Sie hier den interaktiven Wegweiser, der Ihnen in der ersten Zeit nach der Diagnose wertvolle Orientierung geben kann. Welche Therapiemöglichkeiten es bei LHON gibt, besprechen Sie am besten mit Ihrem Arzt oder Ihrer Ärztin. Eine Übersicht mit Fachzentren, die sich auf die Behandlung von LHON spezialisiert haben, finden Sie hier.
- OMIM # 535000. Leber Optic Atrophy. Online unter: https://omim.org/entry/535000?search=LHON&highlight=lhon [letzter Zugriff: 12.11.2020].
- Yu-Wai-Man P et al. Prog Retin Eye Res 2011; 30: 81–114.
- Mascialino B et al. Eur J Ophthalmol 2012; 22: 461–5.
- Jurkute N, Yu-Wai-Man P Curr Opin Ophthalmol 2017; 28(5): 403-409.
- Shemesh A, Margolin E In Stat Pearls Treasure Island (FL). 2018.
- Priglinger C et al. Klin Monatsbl Augenheilkd 2019; 236:1271–1282.
- Poincenot L et al. Ophthalmology 2020; 127: 679–688.
- Rosenberg T et al. IOVS 2016; 57(3): 1370–1375.
- Stenton SL et al. J Clin Invest. 2021; 131(6):e138267.
- Wissinger B. Klin Monatsbl Augenheilkd 2018; 235:1235–1241.
- Yu-Wai-Man P et al. Eye (Lond) 2014; 28:521–537.
- Gueven N Biol Med. 2014; S1: 1–6; 2.
- Kogachi K et al. Mitochondrion 2018; 46: 270-277.
- Rabenstein A et al. Orphanet J Rare Dis 2021; 16: 127.
Symptome
So zeigt sich LHON
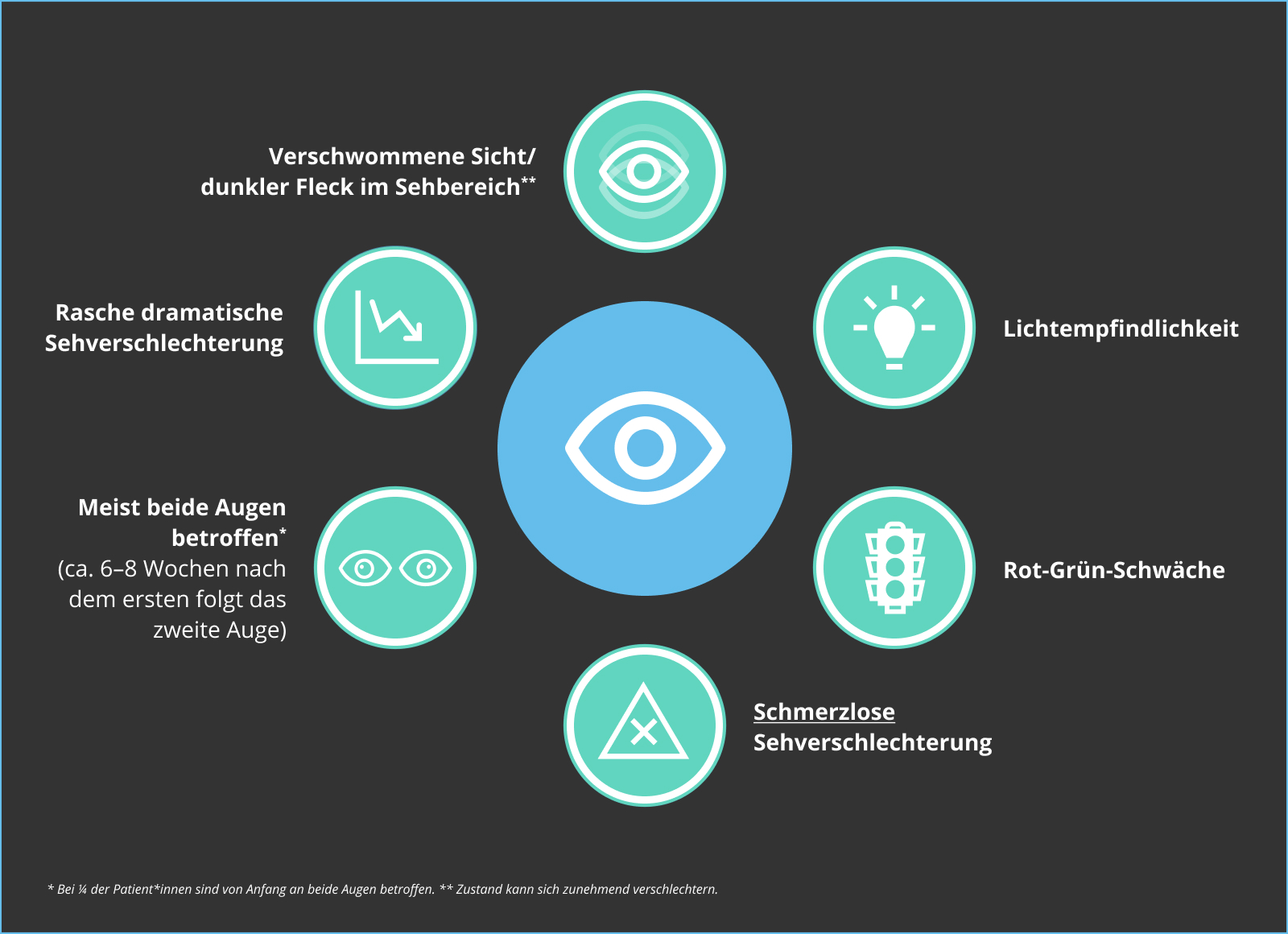
Ein typisches Symptom von LHON ist eine relativ rasche, schmerzlose, unerwartete und fortschreitende Sehverschlechterung, die sich oft zunächst auf ein Auge beschränkt. Das zweite Auge ist meist innerhalb weniger Wochen bis Monate ebenfalls betroffen.1 LHON-Patient*innen bemerken häufig schon früh eine leichte Rot-Grün-Sehschwäche. Diese kann jedoch auch parallel zur Sehverschlechterung auftreten, ebenso wie zu einer erhöhten Lichtempfindlichkeit.2,3 Innerhalb von sechs Monaten nach dem Auftreten erster Symptome ist meist das Maximum der Sehverschlechterung erreicht, danach stabilisiert sich die Sehschärfe.4 Innerhalb eines Jahres nach Krankheitsbeginn ist eine Vielzahl der Patient*innen hochgradig sehbehindert oder nach gesetzlicher Definition blind. 1,2,4-6
Definition von Blindheit
Laut Versorgungsmedizin-Verordnung gelten Menschen als blind, denen das Augenlicht vollständig fehlt. In der Rechtsverordnung ist jedoch zusätzlich festgelegt: „Als blind ist auch ein behinderter Mensch anzusehen, dessen Sehschärfe auf keinem Auge und auch nicht beidäugig mehr als 0,02 (1/50) beträgt oder wenn andere Störungen des Sehvermögens von einem solchen Schweregrad vorliegen, dass sie dieser Beeinträchtigung der Sehschärfe gleichzustellen sind“.6 Man muss also nicht die komplette Sehfähigkeit verlieren, um per Gesetz als blind zu gelten. Auch eine Einschränkung auf 2 % der Sehfähigkeit einer gesunden Person gilt per Gesetz als blind.6
Beteiligung des zweiten Auges
Bei ungefähr einem Viertel der Betroffenen sind von Beginn an beide Augen von der Sehverschlechterung betroffen. Diese Zahl könnte jedoch auch höher liegen, da durch einen Kompensationseffekt die Einschränkung des Sehvermögens auf dem ersten Auge zunächst manchmal nicht bemerkt wird.5 Insgesamt betrifft LHON bei 97 % der erwachsenen Patient*innen innerhalb eines Jahres beide Augen – setzt LHON bereits im Kindesalter ein, ist dies seltener der Fall.5 Bei etwa jedem fünften betroffenen Kind entwickelt sich die Erkrankung schleichend. Teils nimmt die Erkrankung bei Kindern einen asymmetrischen Verlauf, d. h. ein Auge ist betroffen, das andere nicht. Das zweite Auge ist teils erst im Erwachsenenalter betroffen oder bleibt gänzlich verschont.5
LHON Plus
Unter LHON Plus werden Symptome zusammengefasst, die im Zusammenhang mit LHON auftreten können, aber nicht die Augen betreffen. Sie können unterschiedlich sein und sowohl das Nervensystem als auch das Herz betreffen.2,7
Neurologische Symptome
Aufgrund möglicher Überschneidungen zwischen LHON und anderen Erkrankungen, bei denen die Mitochondrien nicht korrekt funktionieren, können LHON-Patient*innen auch neurologische Symptome zeigen. Dazu zählen z. B. Bewegungsstörungen oder eine Enzephalopathie, eine Erkrankung oder Schädigung des Gehirns.8
Herzerkrankungen bei LHON
Bei manchen LHON-Patient*innen können auch Herzerkrankungen wie z. B. Herzrhythmusstörungen auftreten. In einer Studie zeigten 23,2 % der 73 untersuchten Patient*innen mit einem Durchschnittsalter von 30 Jahren Auffälligkeiten am Herzen.9
Harding-Erkrankung
Unter der Harding-Erkrankung versteht man eine Kombination aus LHON und Multipler Sklerose (MS).
Die Betroffenen sind meistens Frauen. Es wird häufig beschrieben, dass zwischen der Einschränkung des Sehvermögens auf dem ersten und dem zweiten Auge viel Zeit vergeht. MS kommt in etwa 5 % der Stammbäume von LHON-Patient*innen vor.10 Umgekehrt entwickeln MS-Patient*innen oft LHON.11 Genetische Untersuchungen zeigen, dass bei 1 bis 15 % der MS-Patient*innen mit frühen, ernsten, ausgeprägten oder beidseitigen Sehstörungen eine LHON-Mutation vorliegt.12 Näheres zur Mutation in der DNA der Mitochondrien bei LHON lesen Sie hier.
- OMIM # 535000. Leber Optic Atrophy. Online unter: https://omim.org/entry/535000?search=LHON&highlight=lhon" [zuletzt aufgerufen 11.07.2024].
- Yu-Wai-Man P et al. Prog Retin Eye Res 2011; 30: 81–114.
- Klopstock T et al. Brain 2011; 134: 2677–286.
- Metz G et al. Acta Ophthalmologica 2014; 92:S253; Poster Presentation (T110), EVER 2014, Nice, France.
- Priglinger C et al. Klin Monatsbl Augenheilkd 2019; 236: 1271–1282.
- Bundesamt für Justiz. Verordnung zur Durchführung des § 1 Abs. 1 und 3, des § 30 Abs. 1 und des § 35 Abs. 1 des Bundesversorgungsgesetzes, unter: https://www.gesetze-im-internet.de/versmedv/anlage.html(zuletzt aufgerufen November 2021).
- Bargiela D et al. Neurosci Lett 2017; pii: S0304-3940(17)30543-8.
- Radelfahr F, Klopstock T. Fortschr Neurol Psychiatr 2018; 86: 584–591.
- Orssaud C. J Neuro-Ophthalmol 2018; 38(4): 466–469.
- Vanopdenbosch L et al. J Neurol. 2000; 247(7):535–43.
- Matthews L et al. J Neurol Neurosurg Psychiatry 2015; 86(5):537–42.
- Palace J. J Neurol Sci. 2009; 286(1-2): 24–7.
- Llòria X et al. Poster Presentation (3362), ARVO 2018, Honolulu, USA.
- Pemp B et al. Graefes Arch Clin Exp Ophthalmol 2019; 257:2751-2757.
Diagnose
So wird LHON festgestellt
Für Augenärzt*innen ist es oft nicht leicht, LHON zu erkennen, weil es sich um eine sehr seltene Erkrankung handelt und es verschiedene andere Erkrankungen gibt, mit denen LHON leicht verwechselt werden kann.1 Zur Diagnose werden daher unterschiedliche augenärztliche Untersuchungen durchgeführt, von denen wir einige im Folgenden näher erläutern.
Funduskopie
Bei einer Funduskopie wird der Augenhintergrund untersucht. Dazu gehören die Netzhaut, die Austrittsstelle des Sehnervs sowie die Blutgefäße. Je nachdem, in welchem Krankheitsstadium sich der*die Patient*in befindet, zeigt sich den Ärzt*innen ein anderes Bild.1
Optische Kohärenztomographie
Die optische Kohärenztomographie (OCT) ist ein nicht invasives Verfahren, bei dem Bilder der Netzhaut im Auge gemacht werden. Diese Methode hilft, verschiedene Augenerkrankungen zu erkennen. Dabei wird ein schwaches Laserlicht verwendet, um die Netzhaut abzubilden. Die Untersuchung ist schmerzfrei. Sie wird genutzt, um die Dicke und die feinen Strukturen der Netzhautschichten zu beurteilen.
Bei der Krankheit LHON kann man mit der OCT je nach Krankheitsphase verschiedene Veränderungen feststellen, wie zum Beispiel die Abnahme der Dicke der Zellschicht der retinalen Ganglienzellen in der Netzhaut im Laufe der Zeit.
Mehr Hintergrundinformationen erhalten Sie hier.
Visuell evozierte Potenziale
Mithilfe dieser Methode wird die Leitfähigkeit von Nervenbahnen im Auge festgestellt. Der zu untersuchenden Person werden hierbei verschiedene visuelle Reize gezeigt, z. B. ein Schachbrettmuster oder Lichtblitze. Gleichzeitig wird über am Kopf befestigte Elektroden die elektrische Aktivität des Gehirns abgeleitet und aufgezeichnet – wie bei einem Elektroenzephalogramm (EEG).6 Bei LHON-Patient*innen zeigen sich im Vergleich zu gesunden Personen starke Unterschiede in den gemessenen Signalen, was auf eine Störung der Sehbahn hindeutet.6,7 Diese Unterschiede entstehen dadurch, dass bei LHON-Patient*innen die Nervenzellen der Netzhaut (retinale Ganglienzellen), die für die Weiterleitung von optischen Signalen ans Gehirn verantwortlich sind, nicht richtig funktionieren können.1
Da LHON leicht mit anderen Erkrankungen verwechselt werden kann, können neben den augenärztlichen Untersuchungen auch weitere Methoden herangezogen werden. Für diese Differenzialdiagnostik, also die Abgrenzung zu anderen Erkrankungen, können neurologische Untersuchungen herangezogen werden:8 Um beispielsweise eine Sehnerventzündung (Optikusneuritis) als Symptom von Multipler Sklerose (MS) auszuschließen, wird eine Magnetresonanztomographie (MRT) des Kopfes und der Augenhöhlen und eine Untersuchung der Gehirn-Rückenmarks-Flüssigkeit (Liquorpunktion) durchgeführt.8,9 Eine Elektroenzephalographie (EEG) kann ebenfalls hilfreich sein.8,9
LHON und Optikusneuritis
Die Optikusneuritis, eine Entzündung des Sehnervs, ist die wichtigste Differenzialdiagnose von LHON.8 Anhand verschiedener Aspekte können sich die beiden Krankheitsbilder in der Regel gut voneinander unterscheiden lassen. Bei der Optikusneuritis betrifft der Sehverlust typischerweise nur ein Auge, zudem haben die Patient*innen Schmerzen beim Bewegen der Augen. Bei ca. 90 % der Patient*innen gehen die Symptome einer Optikusneuritis meist auch ohne Behandlung wieder zurück.10,11 Eine Optikusneuritis tritt außerdem häufig im Zusammenhang mit MS auf.10
Zur Abklärung, ob neben den Augen weitere Organe betroffen sind, ziehen Augenärzt*innen zur Diagnostik auch Kolleg*innen aus der HNO-Medizin, Endokrinologie oder Kardiologie hinzu.8
Eine laborchemische Diagnostik gibt mittels eines Blutbildes z. B. Aufschluss über Leber- und Nierenwerte sowie den Hormon- und Vitaminstatus.8 Auf diese Weise können zum Beispiel Schäden am Sehnerv, die durch Giftstoffe oder Ernährungsmängel wie Vitamin B12-Mangel verursacht werden, ausgeschlossen werden.12
Die genetische Diagnostik bestätigt die klinische (Verdachts-)diagnose LHON letztlich genetisch durch den Nachweis von Mutationen.1 Die ausführliche Untersuchung schließt auch eine Familienanamnese mit ein. Wenn weitere Familienmitglieder an LHON erkrankt sind, kann sich in der Stammbaumanalyse bereits ein Vererbungsschema zeigen.8
Genetische Diagnostik
Die Ursache von LHON liegt in einer Veränderung des Erbmaterials (Mutation) an verschiedenen möglichen Stellen. Die Mutationen können im Erbgut der Mitochondrien (mitochondrialen DNA) oder im Erbgut der Zellen (nukleären DNA) auftreten. Mehr dazu lesen Sie hier.
Eine solche Mutation wird heutzutage in der Regel über zwei verschiedene Methoden nachgewiesen:
Next Generation Sequencing (NGS) ist eine übergeordnete Methode zur Untersuchung der mitochondrialen und der nukleären DNA, die verschiedene Analysen ermöglicht, wie z. B. die Exomsequenzierung und die Gen-Panel-Diagnostik. Während die Exom-Sequenzierung alle kodierenden DNA-Bereiche untersucht, konzentriert sich die Gen-Panel-Diagnostik auf zuvor definierte Gene. Damit können gezielt seltene Mutationen, wie sie bei LHON vorkommen, identifiziert werden.2,4
Welches Probenmaterial ist erforderlich?8
Als Probenmaterial für die genetische Diagnostik von LHON wird üblicherweise Blut abgenommen. In speziellen Fällen können auch Gewebeproben wie beispielsweise Material aus der Mundschleimhaut, Zellen aus dem Urin oder Fibroblasten aus der Haut für die Diagnose herangezogen werden.
Bevor Ihr Erbmaterial analysiert wird, klärt Ihre Ärztin oder Ihr Arzt Sie über das Vorgehen auf und holt Ihre Einwilligung ein.
- Priglinger C et al. Klin Monatsbl Augenheilkd 2019; 236: 1271–1282.
- Carelli V et al. J Neuroophthalmol 2017; 37:371–81.
- Yu-Wai-Man P et al. Prog Retin Eye Res 2011; 30: 81–114.
- Yu-Wai-Man P et al. J Med Genet 2009; 46: 145–8.
- Barboni P et al. Ophthalmology 2010; 117: 623–7.
- Neurologisches Versorgungszentrum Hochsauerland. Visuell evozierte Potenziale(VEP); unter: https://www.neurologie-hsk.de/diagnostik/evozierte-potenziale/visuell-evozierte-potenziale/ (zuletzt aufgerufen Februar 2022).
- Majander A et al. Mitochondrion 2017; 36: 138–149.
- Radelfahr F, Klopstock T. Fortschr Neurol Psychiatr 2018; 86: 584–591.
- Sadun AA et al. Expert Rev Ophthalmol 2012; 7: 251–9.
- Wilhelm H and Schabet M. Dtsch Arztebl Int 2015; 112(37): 616–25.
- Bowling B. Kanski’s Clinical Ophtalmology: A systematic approach, 8th Edition, Butterworth Heinemann, 2015.
- Sadun AA. J Neurol Neurosurg Psychiatry 2002; 72(4): 4235.
- Balducci N et al. Br J Ophthalmol 2016; 100: 1232-37.
Verlauf & Prognose
Wie LHON sich verändert
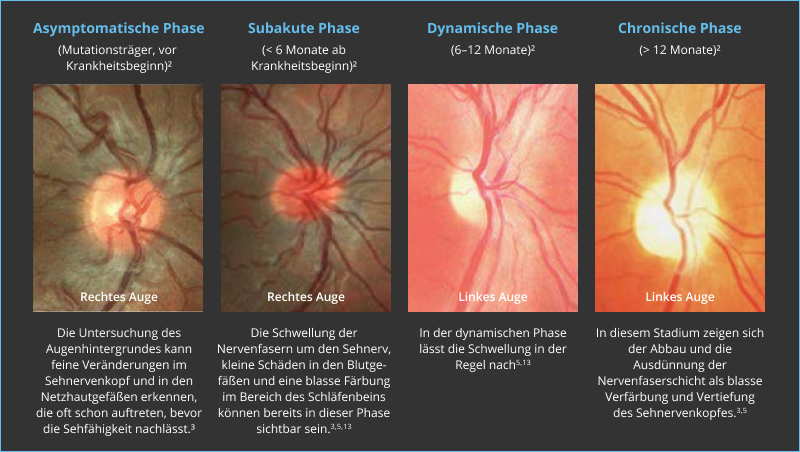
Nach einem internationalen Experten*innen-Kommittee wurden für LHON vier Krankheitsphasen chrakterisiert:10
1: Asymptomatische Phase (vor Ausbruch der Erkrankung)1-4
In der ersten Phase von LHON ist die Sehstärke noch nicht beeinträchtigt. Im zentralen Sichtbereich könnten bei detaillierten Untersuchungen minimale Veränderungen zu bemerken sein, beispielsweise im Rot-Grün-Sehen oder der Wahrnehmung von Kontrasten. Diese Anzeichen führen jedoch zu keiner Beeinträchtigung der Patient*innen.
2: Subakute Phase (< 6 Monate nach Ausbruch)1-6
In dieser Phase setzen die visuellen Symptome ein, es kommt zu einer relativ raschen (subakuten), schmerzlosen Verminderung des Sehvermögens. Die Sehstärke sowie die Fähigkeit zum Farbensehen nehmen ab. In der Mitte des Sichtbereichs kommt es zu Sehstörungen (in der Fachsprache „Gesichtsfeldausfall“, „Zentralskotom“ oder „zentrales Skotom“ genannt). Kurz nach dem ersten Auge kann auch das zweite Auge betroffen sein. Innerhalb von sechs Monaten ist bei den meisten Betroffenen der Punkt erreicht, nach dem sich die Sehschärfe nicht weiter verschlechtert.
3: Dynamische Phase (6–12 Monate nach Ausbruch)1
Die Sehstärke stabilisiert sich, es kann jedoch zu einer weiteren Ausweitung des Gesichtsfelddefekte kommen. Es gibt Patient*innen, die in dieser Phase auch eine spontane Verbesserung des Sehvermögens erfahren können.7 Nach einem Jahr hat das Sehvermögen jedoch bei den meisten erwachsenen Patient*innen auf beiden Augen abgenommen.4 Weitere Infos zur Beteiligung des zweiten Auges erhalten Sie hier.
4: Chronische Phase (> 12 Monate nach Ausbruch)1,4,8
In der chronischen Phase gibt es meist keine weiteren Veränderungen des Sehvermögens. In diesem Stadium sind zahlreiche Patient*innen hochgradig sehbehindert oder gemäß der gesetzlichen Definition blind. Wissenswertes zu der Definition von Blindheit lesen Sie hier.
Prognose
Es gibt Patient*innen, bei denen eine spontane Verbesserung des Sehvermögens auftritt.4 Welche Faktoren eine spontane Verbesserung auslösen können, ist bislang jedoch unbekannt. Am wahrscheinlichsten ist ein Rückgang der Symptome innerhalb der ersten fünf Jahre nach Krankheitsbeginn.8,9 Tritt LHON bereits in der Kindheit auf, kann die Erkrankung unter Umständen einen günstigeren Verlauf nehmen.4 Falls Sie von LHON betroffen sind, wenden Sie sich für Ihre individuelle Prognose bitte an Ihren Arzt oder Ihre Ärztin.
- Carelli V et al. J Neuroophthalmol 2017; 37:371–81.
- Yu-Wai-Man P et al. Prog Retin Eye Res 2011; 30: 81–114.
- Yu-Wai-Man P et al. J Med Genet 2009; 46: 145–8.
- Priglinger C et al. Klin Monatsbl Augenheilkd 2019; 236: 1271–1282.
- Metz G et al. Acta Ophthalmologica 2014; 92:S253; Poster Presentation (T110), EVER 2014, Nice, France.
- Llòria X et al. Poster Presentation (3362), ARVO 2018, Honolulu, USA.
- Pemp B et al. Graefes Arch Clin Exp Ophthalmol 2019; 257: 2751–2757.
- Gueven N. Biol Med 2014; 1:1–6.
- Carelli V et al. Brain. 2011; 134(Pt 9): e188.
- Carelli V et al. J Neuroophthalmol 2017; 37: 371–381.