Clone of Über Raxone®
Therapie & Nebenwirkungen
Therapie mit Raxone®
Idebenon
Idebenon (Raxone®) stellt den einzigen zurzeit zugelassenen medikamentösen Therapieansatz bei LHON dar.1 In Studien konnte gezeigt werden, dass Idebenon eine Wiederherstellung der Sehschärfe fördern und einen weiteren Visusverlust verhindern kann.1,2 Einem internationalen Expertenkonsens von 2017 zufolge sollte allen Menschen mit LHON innerhalb des ersten Jahres nach dem Symptombeginn eine Idebenon-Therapie angeboten werden.3 Mittlerweile sprechen neuere Daten dem Wirkstoff aber auch einen therapeutischen Nutzen in der späten, chronischen Krankheitsphase zu, indem lebensfähige, aber inaktive retinale Ganglienzellen (RGZ) auch noch weit nach Krankheitsbeginn reaktiviert werden können.4,5

Wie wird Idebenon angewendet?
Idebenon zeichnet sich durch ein einfaches Einnahmeschema und ein gutes Sicherheits- und Verträglichkeitsprofil aus.1,2
Seit 2015 ist der Wirkstoff Idebenon (Raxone®) von der Europäischen Arzneimittel Agentur (EMA) zur LHON-Behandlung zugelassen.1 Zulassungsgemäß dürfen jugendliche LHON-Patient*innen ab zwölf Jahren und Erwachsene behandelt werden.1
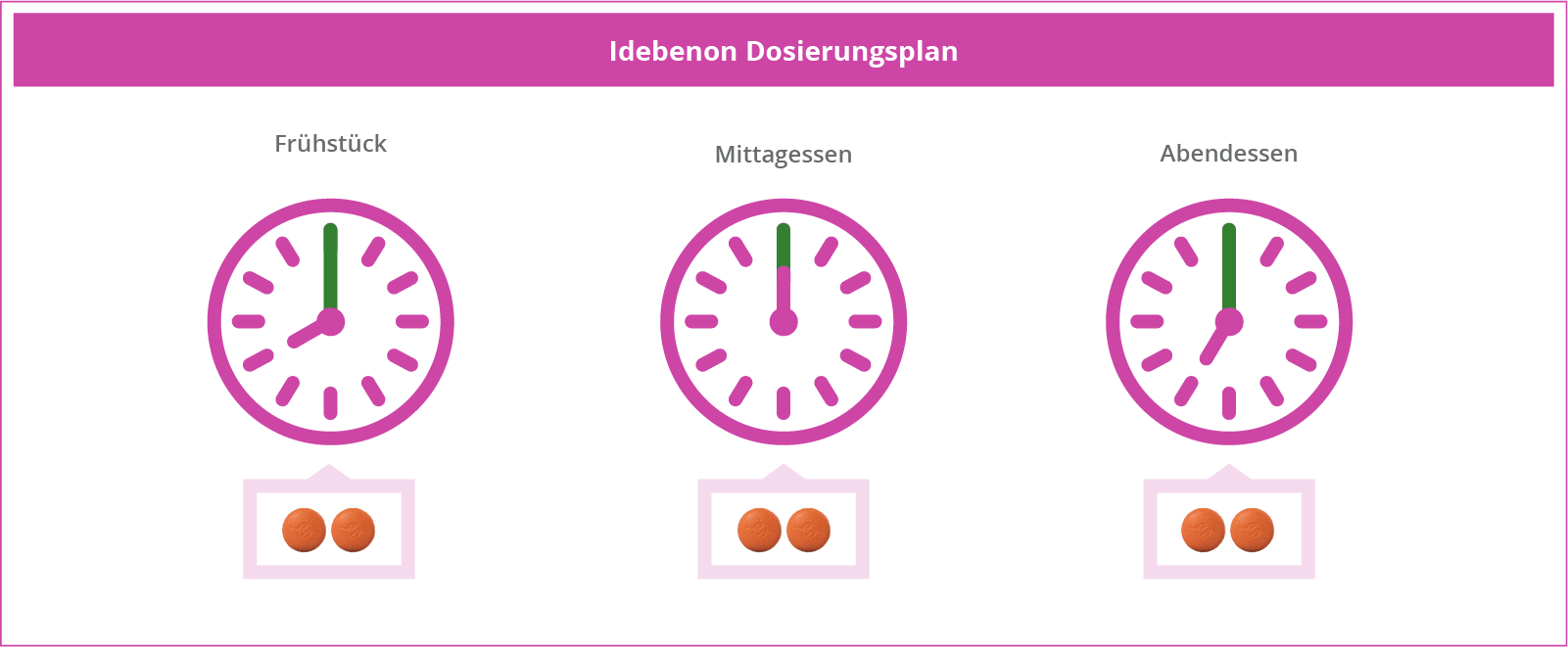
Idebenon wird oral und unzerkaut in einer Dosierung von 900 mg pro Tag eingenommen – aufgeteilt in drei Dosen à 300 mg Wirkstoff (Abb. 2).1 Aufgrund der lipophilen Eigenschaft Idebenons sollte Raxone® zur besseren Resorption zusammen mit einer (fetthaltigen) Mahlzeit eingenommen werden.1,6
Verträglichkeit von Idebenon
Idebenon hat ein gutes Sicherheits- und Verträglichkeitsprofil.2 Die am häufigsten berichteten Nebenwirkungen von Idebenon sind leichte bis mittelschwere Diarrhö (die in der Regel kein Absetzen der Behandlung erforderlich macht), Nasopharyngitis, Husten und Rückenschmerzen.1 Eine vollständige Auflistung der Nebenwirkungen ist in der Fachinformation zu finden.
Responder und Nonresponder
Studien zufolge kann eine Therapie mit Idebenon die Sehkraft von LHON-Patient*innen relevant verbessern.7-9 Es konnte gezeigt werden, dass etwa die Hälfte der Patient*innen von der Therapie profitieren können.2,10 Laut internationalem Expertenkonsens von 2017 sollte allen Menschen mit LHON innerhalb des ersten Jahres nach Symptombeginn eine Idebenontherapie angeboten werden.3 Die Wirksamkeit der Langzeittherapie mit Idebenon in der realen klinischen Praxis wurde in einem Expanded Access Programm (EAP) untersucht. Diese retrospektive, multizentrische, nicht-kontrollierte open-label Analyse schloss 111 LHON-Patient*innen ein, die innerhalb eines Jahres vor Aufnahme in das Programm Symptome zeigten. Die Wirksamkeit von Idebenon wurde erfasst als Anteil der Patient*innen, der eine klinisch relevante Verbesserung (Clinically Relevant Recovery, CRR) oder eine klinisch relevante Stabilisierung (Clinically Relevant Stabilization, CRS) der Sehschärfe erfuhr.2 Im EAP wurden Responder mit klinisch relevanter Verbesserung definiert als Patient*innen mit einer Verbesserung der Sehschärfe von off-chart auf mindestens 5 Buchstaben on-chart oder mit einer On-Chart-Verbesserung von mindestens 10 Buchstaben auf der ETDRS-Tafel.2 Aktuelle Daten daraus zeigten, dass eine längere Behandlungsdauer zu mehr Respondern führt.2 Dabei profitierten 92,5 % der Patient*innen mit Verbesserung nach einer Behandlungsdauer von 24 Monaten. In Einzelfällen trat eine Verbesserung der Sehschärfe auch erst nach 30 Monaten Therapiedauer ein.2 Nach Beginn des therapeutischen Ansprechens kann unter Langzeittherapie mit Idebenon zudem eine weitere Verbesserung der Sehschärfe erreicht werden.2 Nach Erreichen eines Plateaus (Sehschärfestabilisierung) sollte die Idebenongabe noch etwa ein Jahr lang fortgesetzt werden.3 Ein detailliertes Therapieschema finden Sie unter Anwendung.
Die bisherigen Daten konnten zeigen: Je länger die Behandlungsdauer ist, desto höher ist die Chance auf ein Therapieansprechen und auch auf eine weitere Verbesserung der Sehschärfe.2
Der richtige Zeitpunkt
Die Idebenongabe sollte möglichst früh im ersten Jahr nach Symptombeginn begonnen werden, um die schädigenden Einflüsse des oxidativen Stresses möglichst gering zu halten.3 Trotzdem können auch Patient*innen in der chronischen Krankheitsphase (> 1 Jahr nach Symptombeginn) von einer Idebenontherapie profitieren und eine deutliche Verbesserung der Sehschärfe erreichen.4,5 Auch erste Ergebnisse für Idebenon bei chronischen LHON-Patient*innen mit Krankheitsbeginn vor > 5 Jahren deuten darauf hin, dass lebensfähige, aber inaktive RGZ lange nach Krankheitsbeginn reaktiviert werden können.5
Nadir und Therapieadhärenz
Um eine gute Therapieadhärenz möglich zu machen, muss der Patient oder die Patientin darauf vorbereitet werden, dass möglicherweise Geduld nötig ist, bis eine Verbesserung der Sehstärke eintritt. Auch bei Respondern kann es sein, dass sich die Sehkraft unter der Behandlung mit Idebenon zunächst verschlechtert (Nadir). Dies betrifft in erster Linie Patient*innen, die innerhalb des ersten Jahres mit der Therapie beginnen. Nach durchschrittenem Nadir kann ggf. eine Erholung des Visus einsetzen.2 Der Nadir ist häufig auch im natürlichen Verlauf – ohne Idebenontherapie – zu beobachten.11
Unterstützende Maßnahmen
An LHON erkrankte Personen müssen adäquat mit vergrößernden Sehhilfen versorgt werden.6 Zudem sollten Betroffene auf weitere einfach verfügbare Hilfsmittel hingewiesen werden. So kann zum Beispiel ein Smartphone mit der entsprechenden App visuelle Informationen in akustische umwandeln. Weitere Hilfsmittel werden im Patientenbereich auf der Seite Alltagstipps erläutert. In Anbetracht des deutlichen Einschnitts in die Lebensqualität der LHON-Patient*innen empfiehlt es sich auch, die Möglichkeiten der psychologischen Unterstützung für Betroffene und Familienangehörige gemeinsam zu erörtern. Zur Unterstützung der sozialen Rehabilitation sollte zudem die Kontaktaufnahme zu einer Selbsthilfegruppe gefördert werden. Geeignete Ansprechpartner sind beispielsweise unter www.lhon-deutschland.de oder www.pro-retina.de zu finden. Zum Thema der medizinischen und beruflichen Rehabilitation stehen Rehakliniken mit ophthalmologischem Schwerpunkt beratend zur Verfügung und bieten häufig auch praktische Hilfe bei der Antragstellung.
Triggerfaktoren
Das Rauchen von Tabakprodukten zählt nachweislich zu den Triggerfaktoren, die die Konversion von asymptomatischen zu symptomatischen Mutationsträger*innen begünstigen und die Ausprägung der Krankheitssymptome verstärken können.12,13 Starker Alkoholkonsum hat sehr wahrscheinlich ähnliche ungünstige Auswirkungen. Betroffenen sollte daher dringend geraten werden, mit dem Rauchen aufzuhören und ihren Alkoholkonsum einzuschränken.6,12,14 In Einzelfallberichten wurden zudem viele weitere auslösende Faktoren beschrieben, wie z. B. Östrogenmangel, Traumata, antiretrovirale Therapie oder Anämie.15 Auch sollten bestimmte Antibiotika und andere Medikamente, die die mitochondriale Funktion beeinflussen können, nach Möglichkeit gemieden werden.6,12
Ernährung
LHON-Patient*innen profitieren von einer ausgewogenen, obst- und gemüsereichen Kost. Vor allem die Vitamine A, C und E sowie das Spurenelement Selen gelten als wirksame Antioxidantien und können freie Radikale neutralisieren.16 Aktuelle Untersuchungen weisen darauf hin, dass eine kalorienreduzierte ketogene Diät möglicherweise günstige Effekte auf die bioenergetische Kapazität der Mitochondrien hat.17 Weitere Studien sind jedoch nötig, um diese Hinweise zu untermauern.
LHON Register
Das Deutsche Netzwerk für mitochondriale Erkrankungen mitoNET bietet allen Betroffenen die Möglichkeit, sich in das Patient*innenregister mitoREGISTRY eintragen zu lassen. Auch PRO RETINA Deutschland e. V. bietet diese Möglichkeit. So können Menschen mit einer Mitochondriopathie wie LHON aktiv die Erforschung ihrer Erkrankung unterstützen und langfristig die medizinische Versorgung verbessern.
- Fachinformation Raxone®, Stand August 2020.
- Catarino C et al. J Neuroophthalmol 2020; 40: 558–65.
- Carelli V et al. J Neuroophthalmol 2017; 37: 371–381.
- Pemp B et al. J Clin Med. 2021 4;10(1):151.
- Pemp B et al. Graefes Arch Clin Exp Ophthalmol 2019; 257: 2751–2757.
- Priglinger C et al. Klin Monatsbl Augenheilkd 2019; 236: 1271–1282.
- Bartsch V et al. J Med Drug Rev 2016; 6: 35–49.
- Klopstock T et al. Brain 2011; 134: 2677–286.
- Klopstock T et al. Brain 2013; 136: e230.
- Carelli V et al. Brain 2011; 134(Pt 9): e188.
- Metz G et al. Poster Presentation (T110), EVER 2014, Nice, France.
- Sadun AA et al. Clin Exp Ophthalmol 2013; 41: 702–712.
- Rabenstein A et al. Orphanet J Rare Dis 2021; 16: 127.
- Joshi S et al. BMJ Case Rep 2019; 12(3): e228337
- Dimitriadis K et al. Orphanet Journal of Rare Diseases 2014; 9: 158.
- PRO RETINA Deutschland e. V. LHON - Lebersche Hereditäre Optikus Neuropathie Behandlung, unter: https://www.pro-retina.de/netzhauterkrankungen/lhon/behandlung (zuletzt aufgerufen Februar 2022).
- Hage R et al. Front Neurol 2021; 12: 651639.
Wirkstoff & Wirkmechanismus
Wirkstoff
Wirkstoff
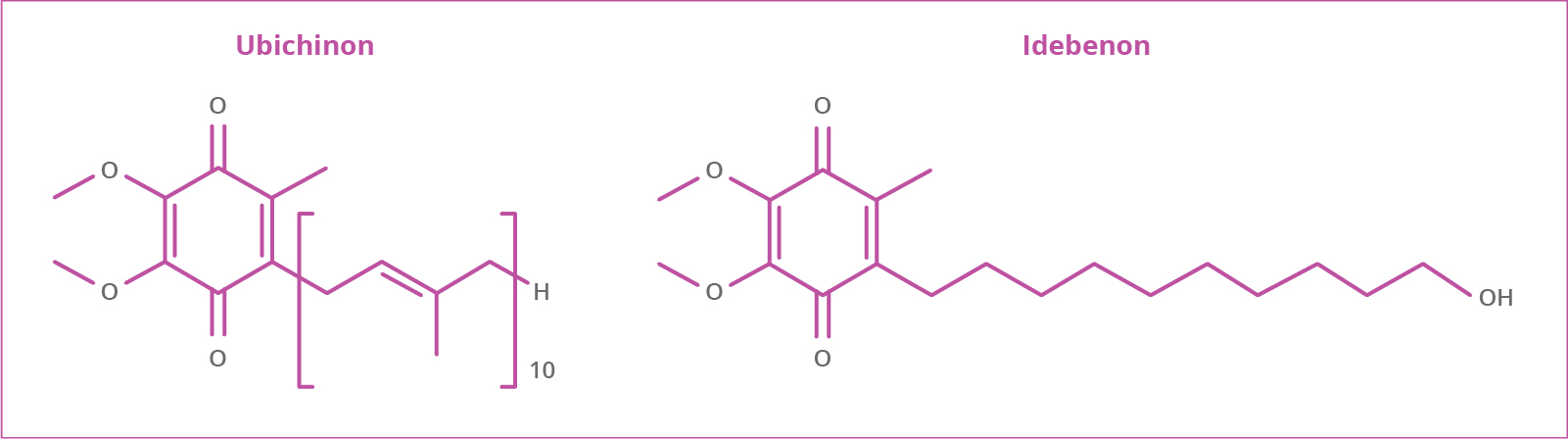
Der Wirkstoff Idebenon (Raxone®) ist – wie auch Ubichinon (Coenzym Q10) – ein Benzochinon.1-3 Ubichinon ist ein normaler Bestandteil der mitochondrialen Atmungskette. Ebenso wie Ubichinon wirkt Idebenon als Antioxidans und Radikalfänger.1-3 Anders als Ubichinon kann Idebenon allerdings in seiner reduzierten Form die äußere Mitochondrienmembran durchdringen und dort im Pendelbetrieb als Elektronen-Shuttle zwischen dem bei LHON zumeist blockierten Komplex I und Komplex III der Atmungskette fungieren.1-3 Da Idebenon die Blut-Hirn-Schranke überwinden kann, erreicht es auch die Mitochondrien der retinalen Ganglienzellen.4
Chemische Struktur und Aktivierung von Idebenon
Idebenon und Ubichinon weisen die gleiche redoxaktive Benzochinon-Struktur auf.4 Ubichinon ist lipophil, Idebenon dagegen jedoch amphiphil.1-3 Die lipophile Seitenkette von Idebenon ist deutlich kürzer als die von Ubichinon und Idebenon besitzt eine endständige Hydroxylgruppe, wodurch sich seine Löslichkeit erhöht und Idebenon die mitochondriale Membran in beide Richtungen passieren kann.3,4 Weitere molekulare Eigenschaften von Idebenon und Ubichinon sind in Tabelle 1 gegenübergestellt.
Idebenon muss im Zytoplasma der Zellen zunächst durch das induzierbare Enzym NADH-Chinon-Oxidoreduktase 1 (NQO1) reduziert und somit aktiviert werden.3 Erst dadurch kann Idebenon als Antioxidans wirken und die äußere Mitochondrienmembran leicht durchdringen, was für den Wirkmechanismus Idebenons von zentraler Bedeutung ist.3
| Molekulare Aktivität | Idebenon | Ubichinon |
| Lipophil2 | + | ++ |
| Membranlokalisation2 | + | ++ |
| Elektronenakzeptor5 | + | + |
| Hydrophil2 | + | |
| Zytoplasmatische Lokalisation2 | + | |
| Fähigkeit, die Membran zu durchdringen2 | + | |
| Einfluss auf den ROS-Spiegel im Zytosol5 | + | |
| Einfluss auf das ATP-Level in betroffenen Mitochondrien5 | + |
Wirkmechanismus
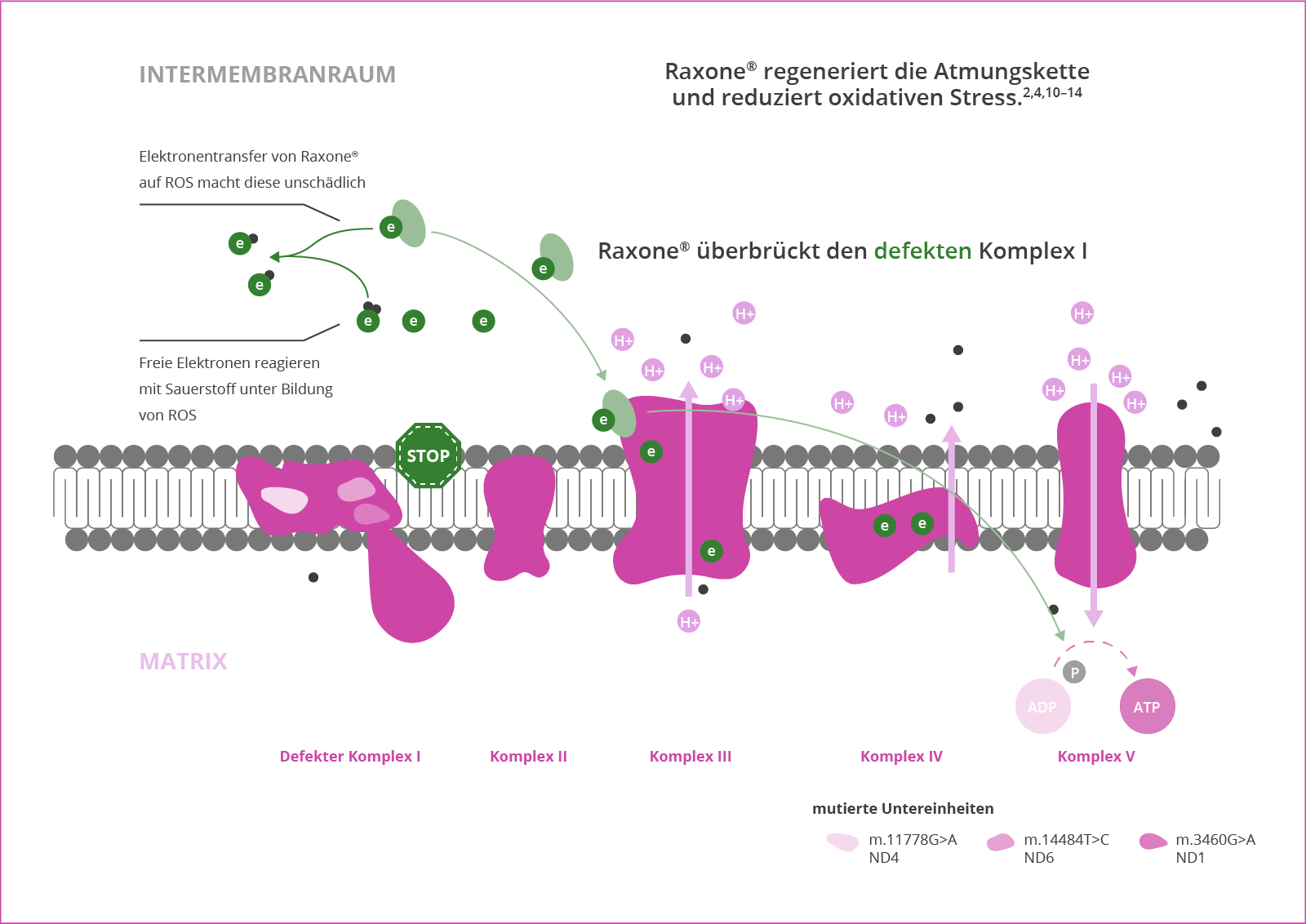
Erreicht die reduzierte Form Idebenons die Mitochondrienmatrix, wird es durch Komplex III an der inneren Mitochondrienmembran reoxidiert.3 Somit entsteht ein Pendelbetrieb vom Zytoplasma zur inneren Mitochondrienmembran und zurück: Idebenon transportiert beständig Elektronen von NQO1 auf Komplex III. Dieser Elektronenfluss sorgt dafür, dass der bei LHON defekte Komplex I überbrückt werden kann und trotz des Defekts Elektronen von Komplex III auf Cytochrom c übertragen werden können.3 Dadurch wird die ATP-Produktion an Komplex V teils wiederhergestellt.6
Der bei LHON vorliegende Gendefekt führt zu einer Funktionsstörung in der Atmungskette.7,8 Durch seinen Wirkmechanismus kann Idebenon die Atmungskette regenerieren, indem es freie Elektronen wieder in die Atmungskette einschleust.1,5,6 Idebenon schützt zudem vor oxidativem Stress: Es wird vermutet, dass der Wirkstoff durch seine Elektronen-Transport-Funktion zu einer Neutralisierung und somit Entgiftung radikaler Sauerstoffspezies (ROS) in den Mitochondrien führen kann.9

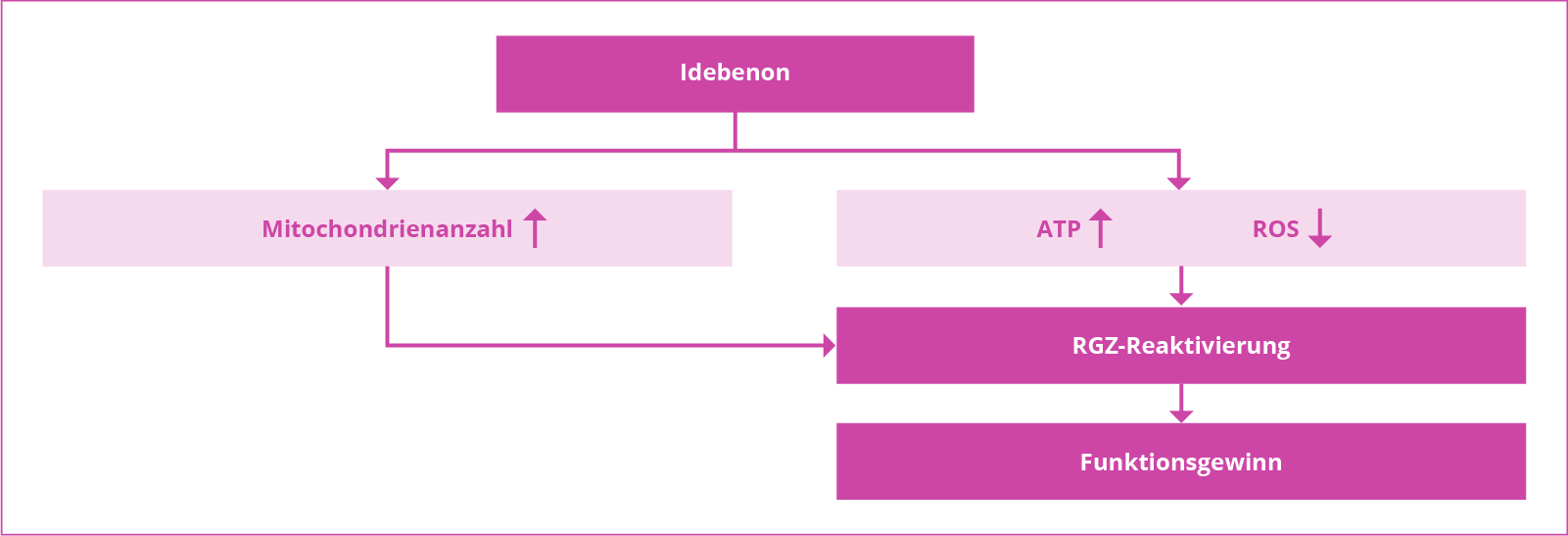
Idebenon beeinflusst die Mitophagie
Des Weiteren konnte im Rahmen von in-vitro Versuchen gezeigt werden, dass Zellen von LHON-Patient*innen mit der mt-DNA-Mutation m.13051G.A eine erhöhte Mitophagie-Rate aufweisen.15 Idebenon konnte die Mitophagie-Rate der Zellen in Experimenten senken und könnte daher zu einer Erhöhung der Mitochondrienzahl bei LHON-Patient*innen beitragen.15 Mehr zur Rolle der Mitochondrien lesen Sie im Abschnitt Pathomechanismus.
Reaktivierung von dormanten retinalen Ganglienzellen (RGZ) durch Idebenon
Daten deuten darauf hin, dass Idebenon möglicherweise vitale retinale Ganglienzellen (RGZ) reaktivieren kann, die sich in einem inaktiven bzw. dormanten Zustand befinden.16 Auch durch diesen Mechanismus könnte eine Wiederherstellung der Sehkraft bei LHON-Patient*innen gefördert werden.16
Ausblick auf die Forschung: Welche weiteren Mechanismen induziert Idebenon?4
Idebenon ist durch seine redoxaktive Benzochinon-Struktur theoretisch dazu in der Lage, als Elektronendonor zu arbeiten und so Radikale zu neutralisieren. Neueren Studien zufolge entfaltet Idebenon seine antioxidative Wirkung jedoch möglicherweise vordergründig über indirekte Mechanismen. Dazu gehört beispielsweise die Hochregulierung der zelleigenen Entgiftungsprozesse (z. B. Proteine wie Superoxid-Dismutase (SOD) oder Glutathion) und die Herunterregulierung des Superoxid-produzierenden Enzyms NADPH-Oxidase 2 (NOX2). Dadurch kann sich der oxidative Stress in den Zellen reduzieren.
Daneben werden weitere Prozesse diskutiert, über die Idebenon seine protektive Wirkung auf die Zellen von LHON-Patient*innen ausübt. Die Inhibition des Proteins p52Shc durch Idebenon und die dadurch ausgelöste nachfolgende Kaskade könnte die Stressresistenz der Zellen erhöhen. In einem präklinischen Tiermodell eines durch Hypoxie/Reperfusion ausgelösten Sehverlusts konnte Idebenon die retinale Expression von Lin28A erhöhen. Dieses Protein reguliert zahlreiche Prozesse der Geweberegeneration – u. a. durch eine erhöhte mitochondriale Funktion. In einem weiteren experimentellen Ansatz konnte Idebenon das Level des Nervenwachstumsfaktors NGF in gealterten Ratten auf das Niveau junger Tiere wiederherstellen. Dies war mit einer verbesserten kognitiven Funktion verbunden.
Welche weiteren molekularen Mechanismen Idebenon über Mitochondrien-fokussierte Mechanismen und antioxidative Wege hinaus induziert, die zu einer schützenden Wirkung bei LHON-Patient*innen führen, ist Gegenstand aktueller Forschung. Zell-protektive Signalkaskaden wie Lin28A sowie der Einfluss von NGF werden als Mechanismen diskutiert.
- Gueven N and Faldu D Intractable Rare Dis Res. 2013; 2(4): 130–5.
- Gueven N et al. Redox Biol 2015; 4:289–295.
- Bartsch V and Mueller-York A J Med Drug Rev 2016; 6:35-49.
- Gueven N et al. Redox Biol 2021; 38: 101812.
- Haefeli RH et al. PLoS One 2011; 6: e17963.
- Erb M et al. PLoS One 2012; 7: e36153.
- Gueven N. Biol Med 2014; S1: 1–6.
- Taylor RW et al. J Med Genet 2003; 40(7): e85.
- Jaber S, Polster BM. J Bioenerg Biomembr 2015; 47(1-2): 111–8.
- Heitz FD et al. PLoS One 2012; 7: e45182.
- Klopstock T et al. Brain 2011; 134: 2677–286.
- Mascialino B et al. Eur J Ophthalmol 2012; 22: 461–465.
- Yu-Wai-Man P et al. Acta Neuropathol 2016; 132(6): 78–806.
- Ravasz D et al. Biochim Biophys Acta (BBA) – Bioenergetics 2018; 1859(9): 909–924.
- Dombi et al. Neurology 2016; 86(20): 1921–3.
- Pemp B et al. J Clin Med 2021 4; 10(1): 151.
Anwendung
Anwendungsgebiet und Dosierung
Raxone® (Wirkstoff Idebenon) ist das erste und einzige zugelassene Arzneimittel zur Behandlung von Sehstörungen bei jugendlichen und erwachsenen Patient*innen mit LHON.1
Raxone® wird oral in Tablettenform (150 g Idebenon pro Tablette) eingenommen. Die empfohlene Tagesdosis beträgt
900 mg Idebenon (3 x 300 mg).1 Die Tabletten sollten morgens, mittags und abends im Ganzen mit Wasser geschluckt werden und dürfen nicht zerteilt oder gekaut werden. Da die Bioverfügbarkeit und Resorption von Raxone® vor allem durch fettreiche Nahrung erhöht wird, sollte das Medikament nach den Mahlzeiten eingenommen werden.1,2

Einnahmedauer
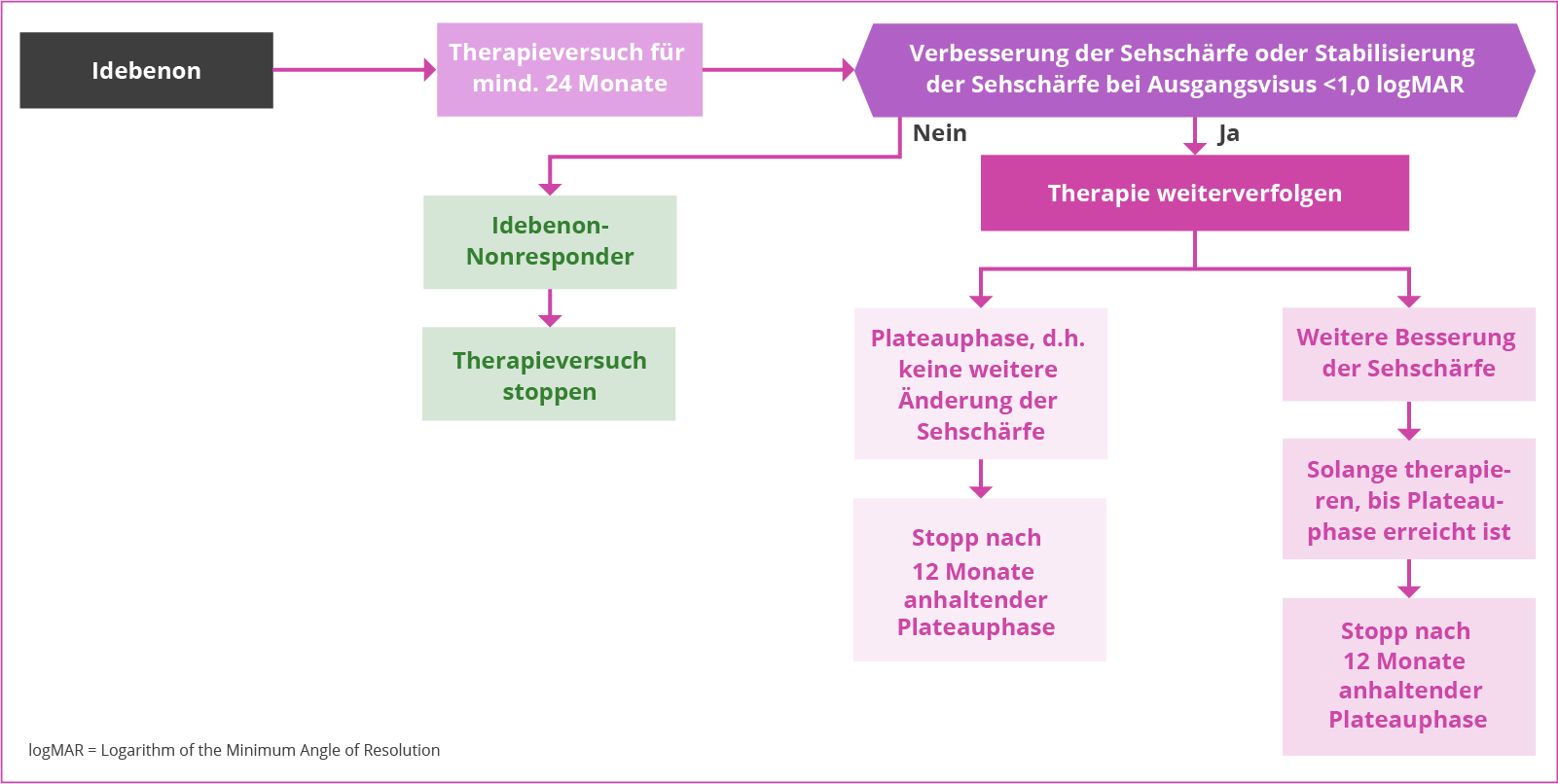
Erkenntnisse aus dem Expanded Access Programm (EAP; retrospektive, multi-zentrische, nicht-kontrollierte open-label Studie) und Experten empfehlen, einen Therapieversuch mit Raxone® mindestens 24 Monate durchzuführen, in einigen Fällen konnte im EAP auch erst nach 30 Monaten Therapie eine erste Verbesserung der Sehschärfe wahrgenommen werden.3,4 Mit zunehmender Behandlungsdauer kann sich das Sehvermögen verbessern: Bei Patient*innen, die ≥ 24 Monate mit Raxone® behandelt wurden, nahm die Anzahl an Respondern in der Population zu. Außerdem konnte bei Patient*innen, die eine Verbesserung bemerkten, das Ausmaß der Verbesserung durch längere Therapie gesteigert werden.4
Besonderer Vorteil für Early Responder
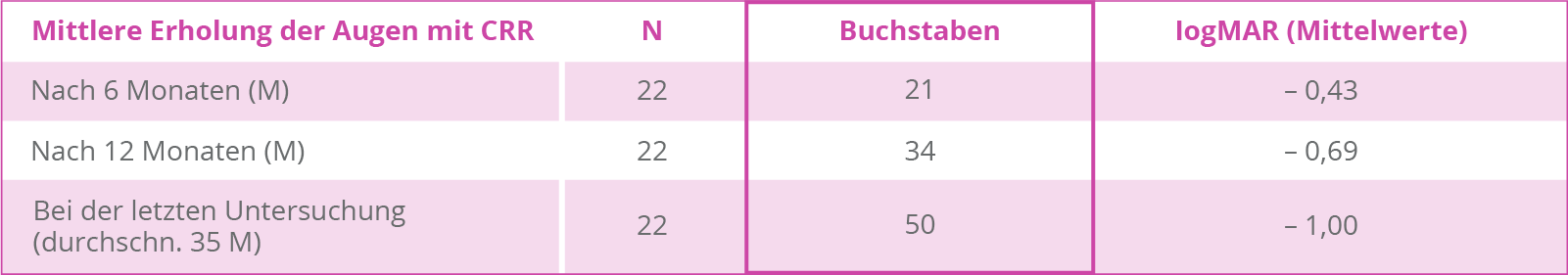
Früh ansprechende Patient*innen (Early Responder) profitierten in einer Studie besonders von einer kontinuierlichen Therapie mit Raxone®. In einer Subgruppe aus dem EAP von 22 Augen mit einer klinisch relevanten Verbesserung (clinically relevant recovery, CRR) nach 6 Monaten führte eine Therapie-Fortsetzung über im Schnitt 35 Monate zu einer größeren Verbesserung der Sehschärfe von 21 Buchstaben nach 6 Monaten und zu 50 Buchstaben nach einer durchschnittlichen Behandlungsdauer von 35 Monaten.4
Auch wenn Early Responder besonders von einer Therapie mit Raxone® profitieren, können Patient*innen auch erst nach 30 Monaten Behandlung ansprechen.3,5 Mehr als 90 % der Responder profitieren von einer Behandlungsdauer von 24 Monaten, in einzelnen Fällen verbesserte sich die Sehschärfe erst nach 30 Monaten Therapie.4 Insgesamt erreichten 46 % der Patient*innen im EAP eine klinisch relevante Verbesserung der Sehschärfe.4
Therapietreue bringt Therapieerfolg
Bei den Patient*innen ist daher Durchhaltevermögen gefragt. Zur Verbesserung der Compliance sollten Patient*innen darauf vorbereitet werden, dass sich ihr Sehvermögen unter Therapie mit Raxone® zunächst verschlechtern könnte bevor es sich verbessert, was dem natürlichen Verlauf der Erkrankung entspricht.6 Mehr zu Nadir und Therapieadhärenz erfahren Sie hier.
Klinische Studien zeigen, dass 30 % der Patient*innen schon nach einer sechsmonatigen Behandlung mit Raxone® eine CRR zeigten.1 Der Anteil der Patient*innen mit Visusverbesserung stieg mit zunehmender Behandlungsdauer an.4 Eine erste Erholung der Sehschärfe lag bei 67,5 % der Patient*innen aus der Responder-Population innerhalb von 12 Monaten Behandlung mit Raxone® vor, nach 24 Monaten profitierten 92,5 % der Responder.4 Weitere Infos zu Respondern und Nonrespondern der Raxone®-Therapie erhalten Sie hier.
Beendigung der Therapie
Eine ausbleibende weitere Visusverbesserung ist der Indikator für die Beendigung der Therapie, die Behandlung mit Raxone® sollte jedoch erst ein Jahr nach Erreichen eines Plateaus der Sehschärfe (Sehschärfestabilisierung) beendet werden.3
Verlaufskontrolle
Die Patient*innen sollten gemäß lokaler klinischer Praxis regelmäßig überwacht werden.1,7 Eine Untersuchung des Visus und des Gesichtsfelds eignen sich als routinemäßige Verlaufsparameter.8 Bei den Kontrollterminen sollte zudem eine Blutuntersuchung durchgeführt werden, die Laborparameter zu Nieren-und Leberwerten beinhaltet.1 Zunächst sollten die Verlaufskontrollen üblicherweise alle drei Monate stattfinden, später alle sechs Monate und alle 12 Monate, wenn sich eine Stabilisierung des Visus eingestellt hat.3
Haltbarkeit und Aufbewahrung
Raxone® ist 5 Jahre haltbar. Es sind keine besonderen Lagerungsbedingungen erforderlich.1 Informationen zu möglichen Nebenwirkungen von Raxone®, Gegenanzeigen und Wechselwirkungen mit anderen Arzneimitteln erhalten Sie hier.
- Fachinformation Raxone®, Stand August 2020.
- Kutz K et al. J Neurol 2009; 256 Suppl 1: 31–5.
- Löffler C. LHON: Aktuelle Therapiedaten und Differenzialdiagnostik in der ärztlichen Praxis. Sonderpublikation in: Der Ophthalmologe 2021; Band 118, Heft 4.
- Catarino CB et al. J Neuro-Ophthalmol 2020; 40: 558–565.
- Metz G et al. Oral Presentation at the 11th Congress of European Neuroophthalmological Society (EUNOS) 2015, Ljubljana (Slovenia). Abstract.
- Metz G et al. Poster Presentation (T110), EVER 2014, Nice, France.
- Klopstock T et al. Brain 2011; 134(9): 2677–86.
- Priglinger C et al. Klin Monatsbl Augenheilkd 2019; 236: 1271–1282.